相关实验
实验承诺函
咨询记录
技术文章

城市
时间
江苏省南京市
2026-05-03 20:03:18
江苏省南京市
2026-05-03 19:00:51
浙江省丽水市
2026-05-03 18:57:01
江苏省南京市
2026-05-03 10:16:32
江苏省徐州市
2026-05-03 04:07:28
江苏省徐州市
2026-05-03 02:08:43
江苏省南通市
2026-05-02 10:32:53
浙江省丽水市
2026-05-02 08:25:09
浙江省丽水市
2026-05-01 17:53:04
江苏省常州市
2026-05-01 17:51:33
TSA 放大技术如何提升检测信噪比?【TSA 检测外包】
2025-09-25 11:45:59
TSA 放大技术怎么选?不同场景下的选型指南与注意事项
2025-09-22 18:18:58
为什么选择TSA放大技术?
2025-09-19 16:42:50
做多重荧光总翻车怎么办?TSA 信号放大 10-1000 倍!mIHC 五标六色实测稳
2025-09-08 18:31:17

蛋白原核表达-从原理到实操超详细教程【蛋白表达】
2025-09-05 10:39:38

攻克蛋白表达难题?原核表达系统解锁高产量、低成本的重组蛋白制备新方案!
2025-09-04 11:55:11

二抗法与TSA 法:免疫荧光实验方法怎么选?看完这篇就懂
2025-09-02 17:26:48
什么是 RNP 法KO细胞株服务?
RNP(核糖核蛋白复合物)法 KO 稳株服务,是将预先组装好的 Cas9 蛋白与向导 RNA(gRNA)形成的 RNP 复合物,通过电穿孔技术精准导入目标细胞,实现特定基因稳定敲除(KO)的专业服务。我们依托优化的 RNP 组装体系与高效电转平台,针对客户需求设计个性化方案,构建遗传背景清晰、表型稳定的 KO 细胞株,为科研与药物研发提供核心实验模型。
RNP 复合物组装:将高活性 Cas9 蛋白与靶向目标基因的特异性 gRNA 在体外进行组装,形成具有高度靶向性的编辑复合物。
电穿孔导入:利用电转仪产生的瞬时电场在细胞膜上形成微孔,使 RNP 复合物高效进入细胞,相比传统病毒转染或质粒转染,大幅提升编辑效率与细胞存活率。
精准基因敲除:进入细胞的 RNP 复合物快速识别靶基因序列并切割,触发细胞内源性 DNA 修复机制(非同源末端连接 NHEJ),最终实现目标基因的稳定敲除。
低脱靶保障:RNP 复合物在细胞内半衰期短(24-48 小时),可快速降解,显著降低长期表达导致的脱靶效应,同时避免外源基因整合带来的基因组干扰
超高精准性:RNP 复合物直接作用于靶序列,无外源 DNA 整合,结合短半衰期特性。
高效转染:电转技术适配多种难转染细胞(如免疫细胞),高于脂质体转染。
快速交付:优化的 RNP 组装-电转-筛选流程,无需等待蛋白表达,稳株构建周期缩短至8-12周。
细胞友好:低电压脉冲设计减少细胞损伤,适合珍贵细胞样本。
广泛适用:覆盖肿瘤细胞、免疫细胞(如 T 细胞、NK 细胞)等 200 + 细胞类型。
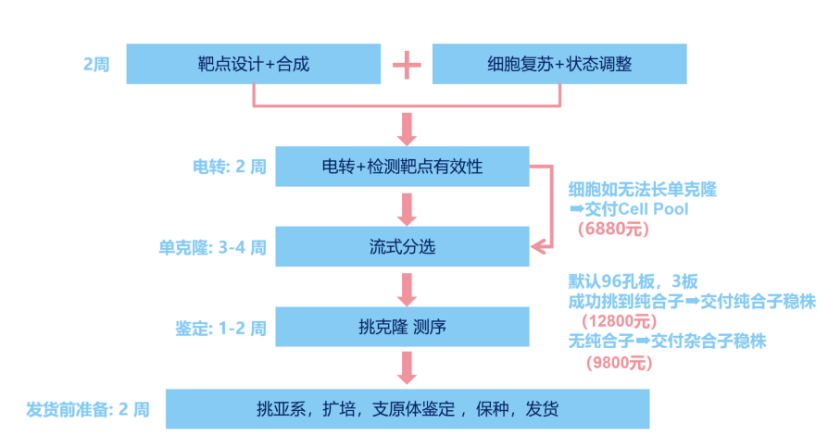
标准化服务流程
1. 需求定制:深入沟通客户研究目标(如基因功能、药物筛选)、靶基因信息及细胞特性(如细胞系 / 难转染程度),提供全面的可行性评估报告与个性化方案。
2. RNP 设计与组装:根据靶基因序列设计2条高特异性 gRNA。
3. 细胞电转与培养:将 RNP 复合物通过电转入细胞,置于专用培养体系中恢复培养,实时监测细胞状态。
4. 单克隆筛选与鉴定:采用流式细胞分选获得单克隆细胞,通过 PCR 扩增靶基因片段、Sanger 测序验证敲除效率,筛选纯合子克隆。
5. 交付与售后:交付合格 KO 细胞株(含冻存管2支)、完整实验报告(含 gRNA 序列、测序结果),提供 1 个月技术支持,解答后续培养与实验疑问。
1. 基因型验证:采用Sanger 测序确认靶基因敲除类型(移码突变 / 片段缺失)
2. 细胞质控:
(1) 支原体检测:PCR 法检测支原体,结果阴性方可交付。
(2) 追溯体系:每批次实验保留检测原始数据,支持结果溯源与重复验证。
(3) 表型验证:可根据客户需求,加做细胞增殖(CCK-8)、凋亡(流式 Annexin V)、功能标志物表达(Western Blot / 流式)等表型变化检测服务。
1. 基因功能研究:构建特定基因 KO 稳株,通过对比野生型与 KO 细胞的转录组、代谢组差异,解析基因在细胞周期、信号通路、疾病发生中的调控机制。
2. 肿瘤研究与药物筛选:针对肿瘤驱动基因(如 EGFR、KRAS)构建 KO 稳株,用于验证药物靶点有效性,或筛选靶向该基因的小分子药物、抗体药物。
3. 细胞治疗研发:在 CAR-T 细胞、iPSC 等细胞治疗领域,通过 RNP 电转敲除 PD-1、TCR 等基因,增强细胞治疗效果,降低免疫排斥风险。
4. 传染病研究:敲除病毒受体基因(如 ACE2、CD4)构建抗病毒细胞模型,用于病毒入侵机制研究及抗病毒药物筛选。
5. 遗传病模型构建:模拟人类遗传病相关基因突变(如囊性纤维化 CFTR 基因、镰状细胞贫血 HBB 基因),建立 KO 细胞模型,助力发病机制研究与基因治疗方案开发。
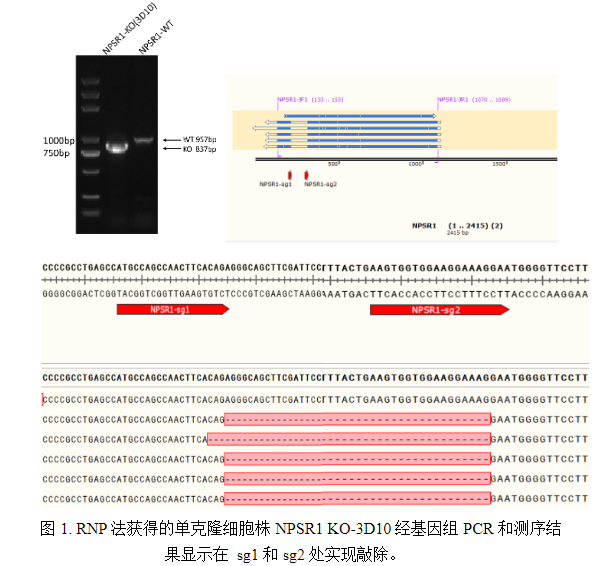
某三甲医院肿瘤研究所需构建结直肠癌细胞KO细胞株(靶基因为NPSR1),传统脂质体转染效率不足30%。我们采用RNP电转法,优化参数后转染效率达80%,8周成功交付KO单克隆纯合子,经团队后期Western blot检测,NPSR1基因敲除率100%。
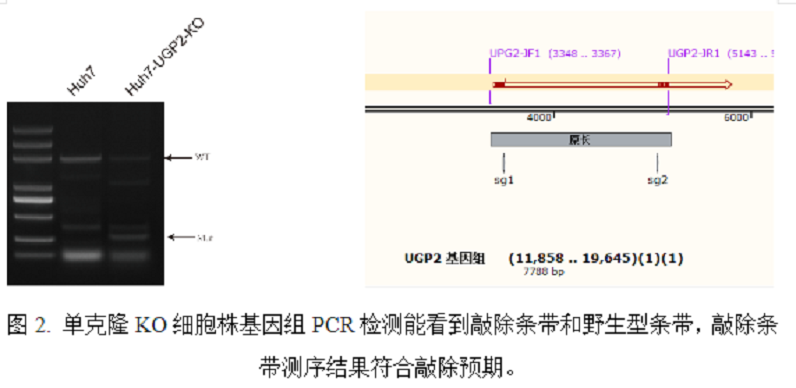
某高校附属医学院肝病研究所需敲除原代肝癌细胞中的UPG基因以进行药筛。我们通过设计2条gRNA与Cas9蛋白组装,并使用RNP电转法在原代肝癌细胞中成功实现了UPG基因的杂合敲除,单克隆细胞存活率100%。
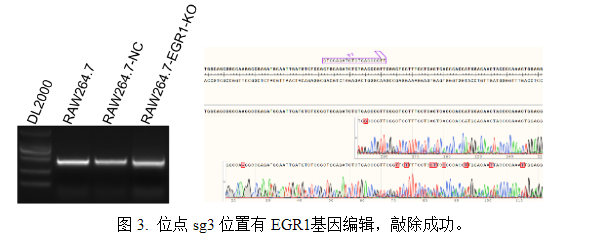
某高校发育生物学团队需在小鼠单核巨噬细胞白血病细胞系(Raw264.7)中敲除EGR1基因,由于细胞半悬浮半贴壁生长,传统脂质体转染及慢病毒法敲除效率低、周期长,我们采用低损伤RNP电转方案,设计3条sgRNA,最终获得 EGR1 KO细胞池(多克隆),团队继续进行单克隆筛选。