案例一
检测服务
案例展示
实验介绍
【应用简介】
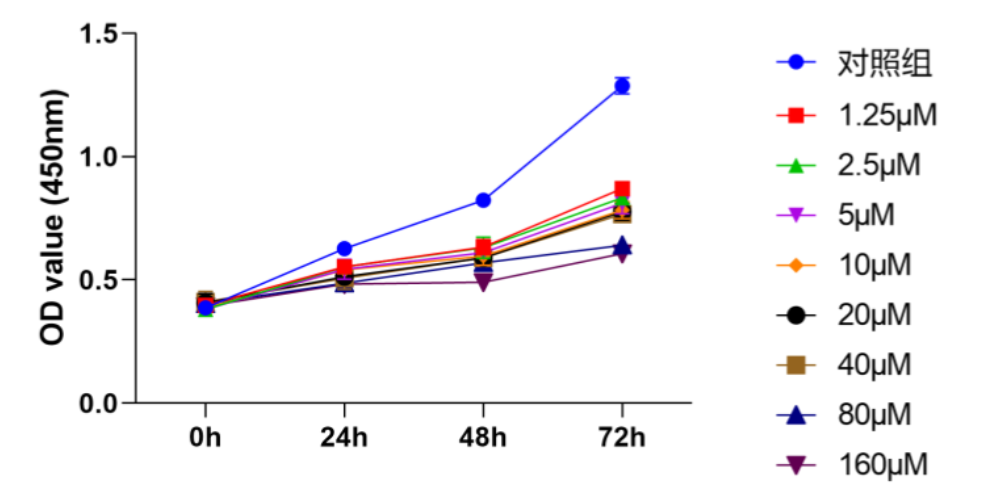
细胞增殖是生物体生长、发育、繁殖和遗传的基础,与细胞凋亡、细胞周期等是肿瘤研究的重要表型,同时也是分子生物学和药理学研究的重要内容。MTT或CCK8是检测细胞增殖的常用手段,可研究药物对细胞的毒性作用;或探究过表达或干扰细胞中某个基因对细胞增殖能力的影响,为进一步研究基因的功能提供依据等。
【MTT技术原理】
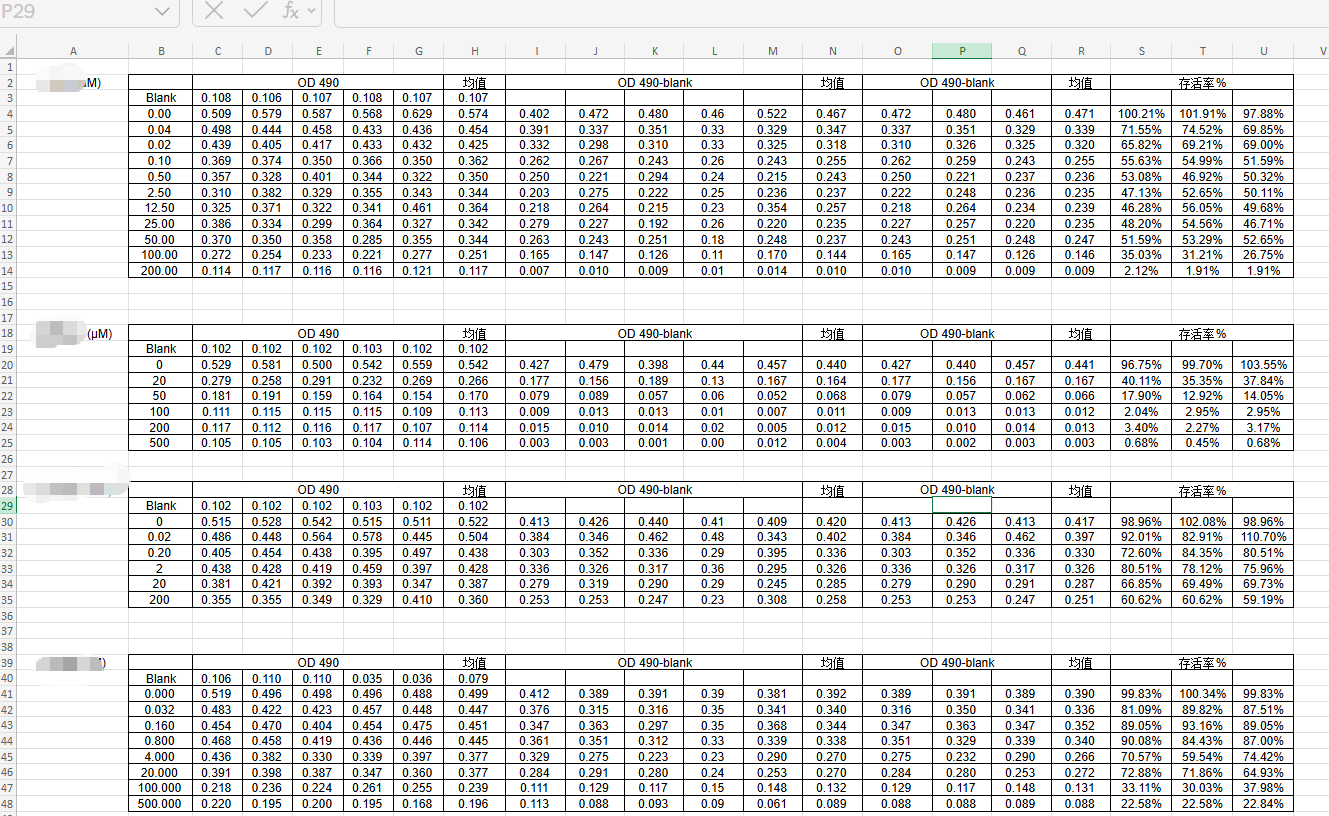
MTT(噻唑蓝),可透过细胞膜进入细胞内,活细胞线粒体中的脱氢酶能使外源性MTT还原为不溶于水的蓝紫色结晶并沉积在细胞中,而死细胞无此功能;结晶物能溶于DMSO中,通过酶联免疫检测仪在490 nm波长处测定其光吸收值,间接反映活细胞数量(一定范围内,OD值越大,细胞活性越强)。
【CCK8技术原理】
CCK-8试剂中的WST-8,可在电子载体1-甲氧基-5-甲基吩嗪鎓硫酸二甲酯(1-Methoxy PMS)的作用下被活细胞线粒体中的脱氢酶还原为具有高度水溶性的黄色甲瓒产物;用酶联免疫检测仪在450 nm波长处测定其光吸收值,可间接反映活细胞量(一定范围内生成的甲瓒物的数量与活细胞的数量成正比)。
【技术总结】
常见问题及注意事项:
1. 铺板密度不合理,均匀度不一致;
2. 实验分组不严谨;
3. 实验设置时间点不合理;
4. MTT或CCK8加样时注意事项不明确;
5. 血清等影响:高浓度血清或药物颜色会影响试验孔的吸光度值;
6. 边缘效应:边缘孔的水分挥发较快,药物易被浓缩。
【交付标准】
1. 实验报告
2. 真实实验结果
3. 原始图片
4. 实验原始数据
5. 剩余物料在周期内可返还(超过周期,不予返还)
技术文章
更多文章咨询记录
| 城市 | 咨询内容 | 时间 | |
|---|---|---|---|
| 上海市 | 咨询细胞活力(CCK8/MTT法)服务相关 | 2026-05-21 13:59:00 | |
| 上海市 | 咨询细胞活力(CCK8/MTT法)服务相关 | 2026-05-21 13:59:00 | |
| 上海市 | 咨询细胞活力(CCK8/MTT法)服务相关 | 2026-05-21 12:56:00 | |
| Hauts-de-FranceNord | 咨询细胞活力(CCK8/MTT法)服务相关 | 2026-05-21 12:08:00 | |
| 广东省广州市 | 咨询细胞活力(CCK8/MTT法)服务相关 | 2026-05-21 10:59:00 | |
| 江苏省扬州市邗江区 | 咨询细胞活力(CCK8/MTT法)服务相关 | 2026-05-21 07:49:00 | |
| CaliforniaCupertino | 咨询细胞活力(CCK8/MTT法)服务相关 | 2026-05-20 19:54:00 | |
| GeorgiaAtlanta | 咨询细胞活力(CCK8/MTT法)服务相关 | 2026-05-20 19:41:00 | |
| 北京市 | 咨询细胞活力(CCK8/MTT法)服务相关 | 2026-05-20 19:06:00 | |
| 江苏省扬州市 | 咨询细胞活力(CCK8/MTT法)服务相关 | 2026-05-20 17:40:00 | |