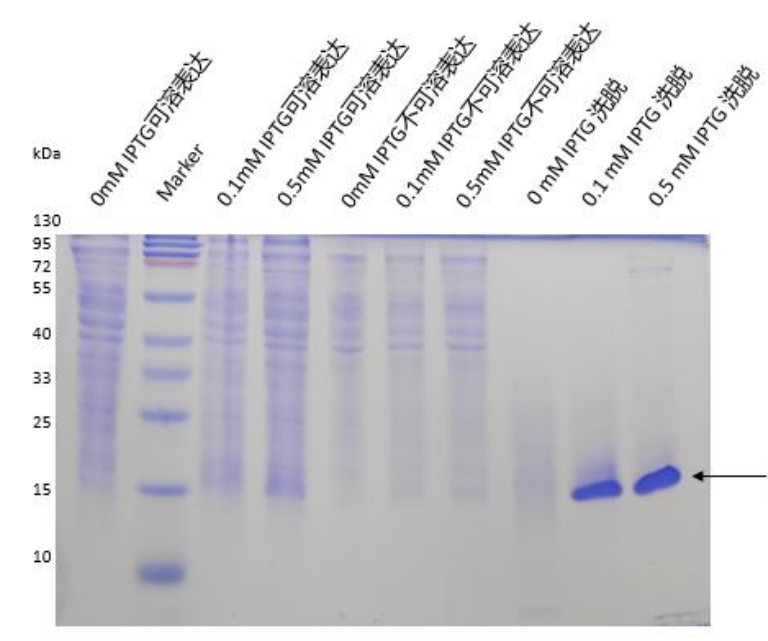
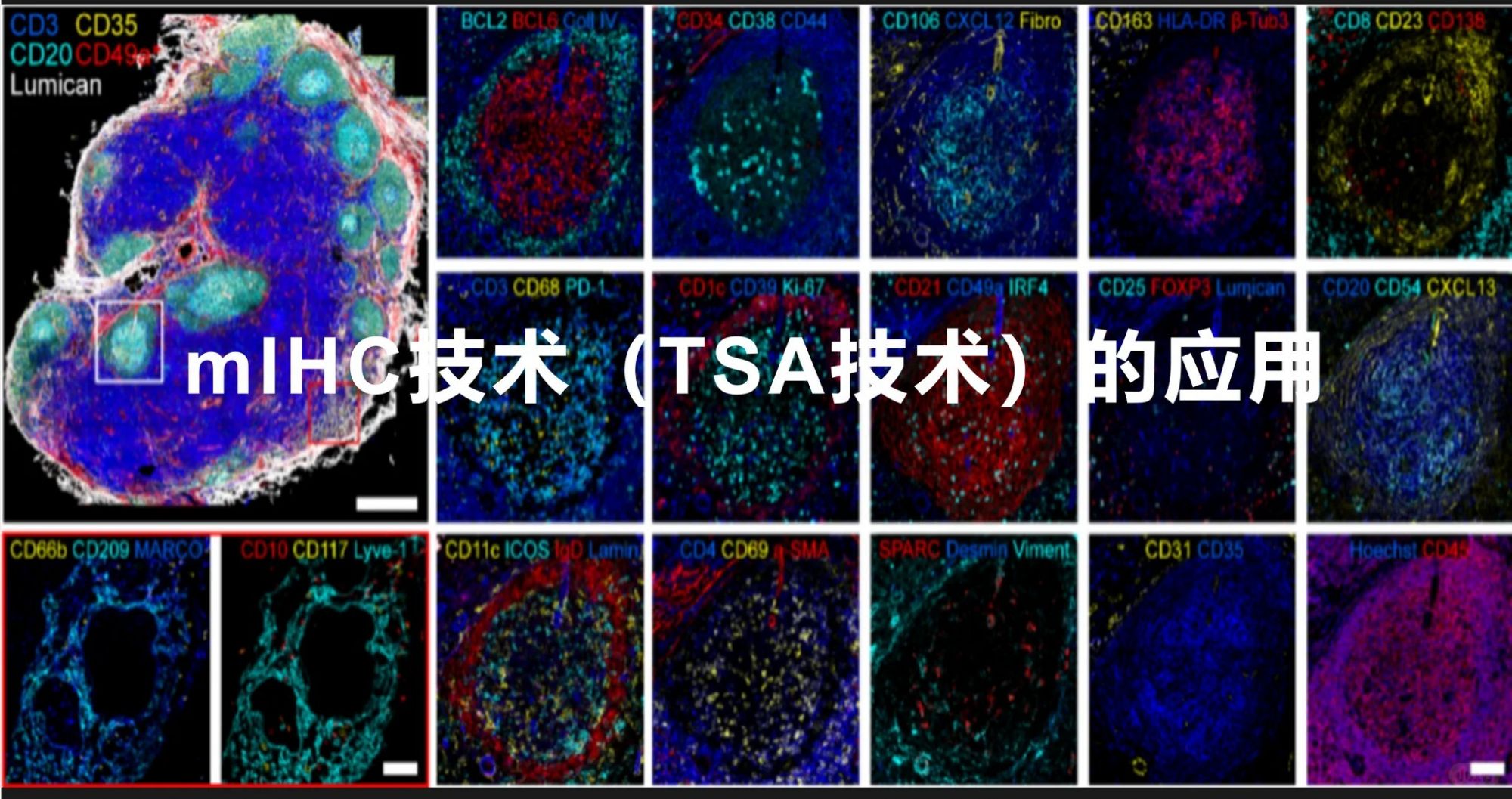
案例一
检测服务
案例展示
技术文章
更多文章咨询记录
| 城市 | 咨询内容 | 时间 | |
|---|---|---|---|
| WashingtonGrant | 咨询KO技术服务服务相关 | 2026-06-07 16:40:00 | |
| 浙江省杭州市 | 咨询TSA(多标IF)技术服务服务相关 | 2026-06-07 16:36:00 | |
| 浙江省杭州市 | 咨询KO技术服务服务相关 | 2026-06-07 16:36:00 | |
| 北京市 | 咨询TSA(多标IF)技术服务服务相关 | 2026-06-07 15:37:00 | |
| 北京市 | 咨询KO技术服务服务相关 | 2026-06-07 15:37:00 | |
| 国外 | 咨询KO技术服务服务相关 | 2026-06-07 12:54:00 | |
| 北京市 | 咨询TSA(多标IF)技术服务服务相关 | 2026-06-07 12:54:00 | |
| 北京市 | 咨询蛋白原核表达服务服务相关 | 2026-06-07 12:54:00 | |
| 河北省张家口市 | 咨询KO技术服务服务相关 | 2026-06-07 12:31:00 | |
| 江苏省连云港市 | 咨询蛋白原核表达服务服务相关 | 2026-06-07 11:47:00 | |