同时还在其余多种肿瘤中,继续对LINRIS的表达进行检测,充分证明LINRIS促癌作用的“普适性”(Fig 1D, F)
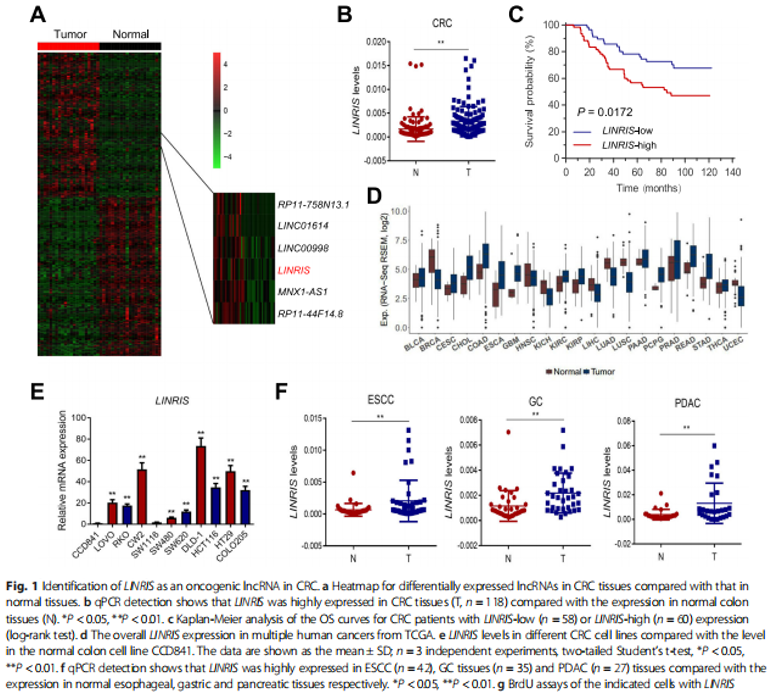
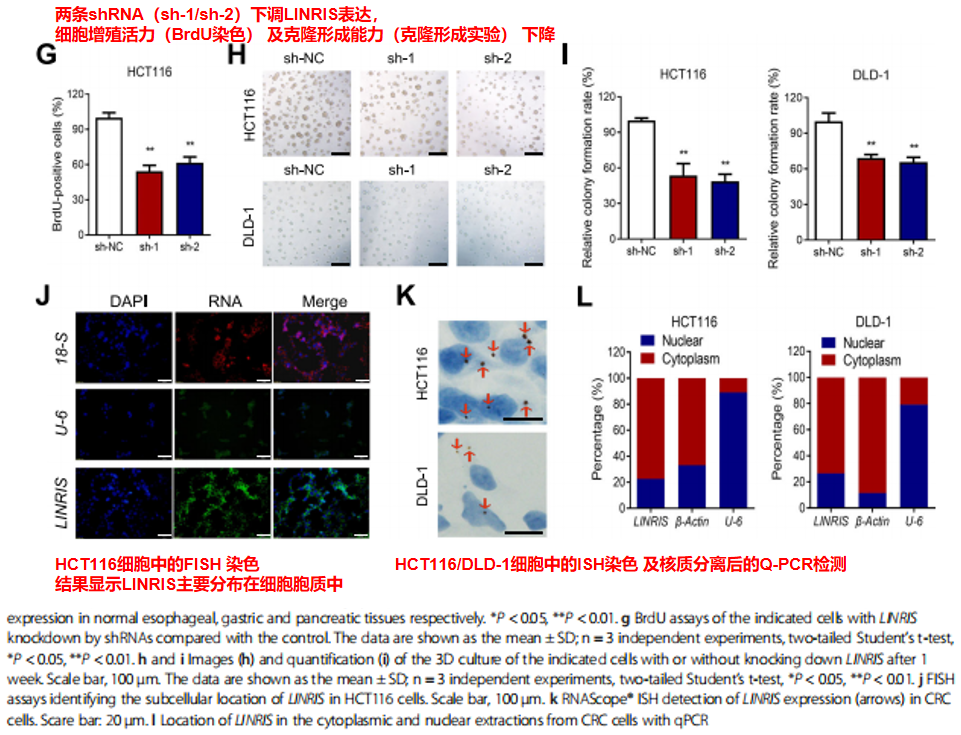
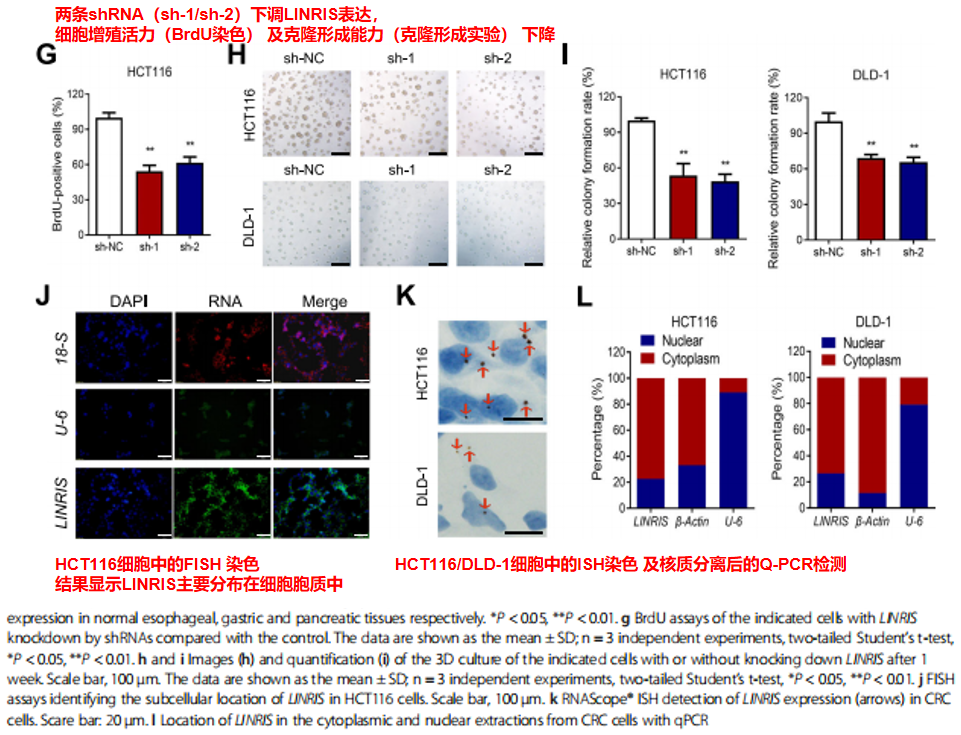
同时,进一步分析了LINRIS在细胞中的具体分布:主要是分布在胞质中,而非胞核中(Fig 1J-L)
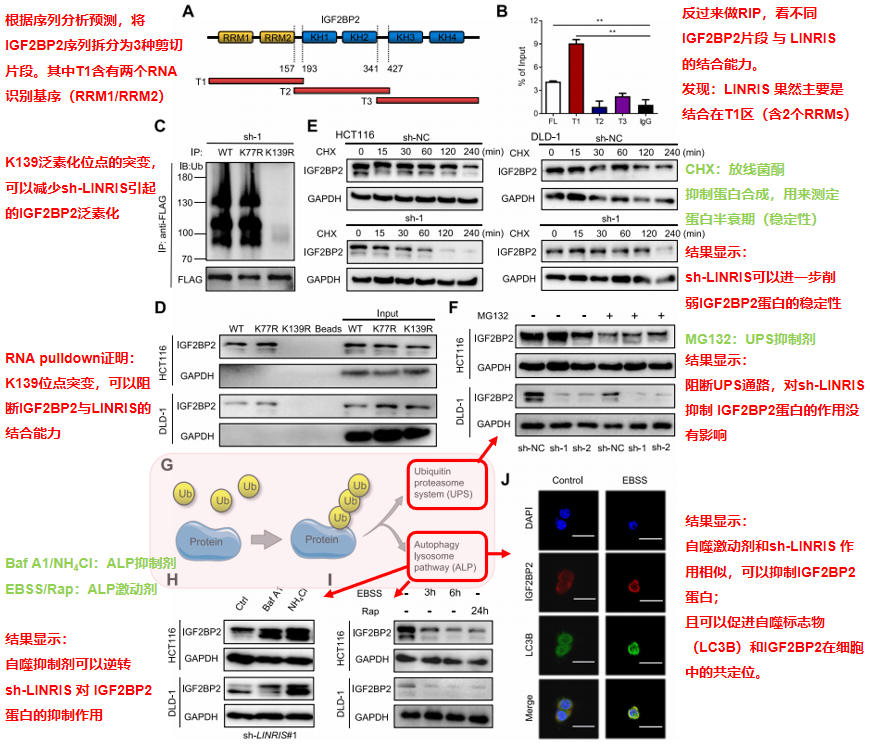
② 然后花式RNA pulldown,先证明IGF2BP2可以与LINRIS结合(Fig 2A, B),再证明IGF2BP2是特异性的与LINRIS结合,而非构建的质粒上其他不相关的元件(Fig 2C, D),接着证明了IGF2BP2既不是与LINRIS的C端,也不是与N端结合(Fig 2E),而是结合在LINRIS序列的 450-640bp位置(但是这么关键的数据,又是在附录里)。
最后在Fig 1E中同样的11株结直肠癌细胞系中检测了IGF2BP2的蛋白含量,并发现其表达规律与LINRIS呈正相关(Fig 2F, G)。而沉默LINRIS,可以下调IGF2BP2的蛋白含量,上调它的泛素化水平(Fig 2H, I)。
其次分析结合后如何调控IGF2BP2的泛素化。IGF2BP2上有两个泛素化位点(K77, K139)。课题组对两个位点进行突变,然后发现,只有当K139位点发生突变后,可以阻断sh-LINRIS对IGF2BP2蛋白泛素化(Fig 3C)以及与IGF2BP2的结合能力(Fig 3D)的调控作用。
泛素化发生后,一般就是直接引起蛋白的降解。所以最后再研究LINRIS调控IGF2BP2泛素化以后,是如何调控IGF2BP2降解的。先用CHX蛋白稳定性检测实验再次证明,sh-LINRIS可以降低IGF2BP2的蛋白稳定性(Fig 3E),即确实可以加速IGF2BP2的降解。又已知泛素化后蛋白降解主要有UPS 和 ALP两条途径。所以最后进行一一验证:加入UPS抑制剂MG132,sh-LINRIS对IGF2BP2蛋白含量的抑制作用没有改变(Fig 3F);而自噬抑制剂却可以明显逆转sh-LINRIS对IGF2BP2蛋白含量的抑制作用(Fig 3H),相反,自噬激动剂则可以像sh-LINRIS一样,促进IGF2BP2的降解(Fig 3I, J)
IGF2BP2下游,就挑了一个IGF2BP2的经典靶点c-Myc,然后因为课题组一直都关注的是代谢功能,所以又挑了几个既是c-Myc下游,又是有氧糖酵解的标志物的基因(GLUT-1, PKM2, LDHA)进行检测验证。
① Q-PCR/WB结果显示 sh-LINRIS可以抑制c-Myc及GLUT-1, PKM2, LDHA的表达,且在临床样本中c-Myc, GLUT-1, PKM2, LDHA的表达与LINRIS的表达均呈正相关(Fig 4A-C)。
糖酵解标志功能 细胞外酸化率(Fig 4D, E)及糖酵解途径代谢产物示踪检测(Fig 4F)结果显示,sh-LINRIS 可以显著抑制结直肠癌细胞的糖酵解过程。
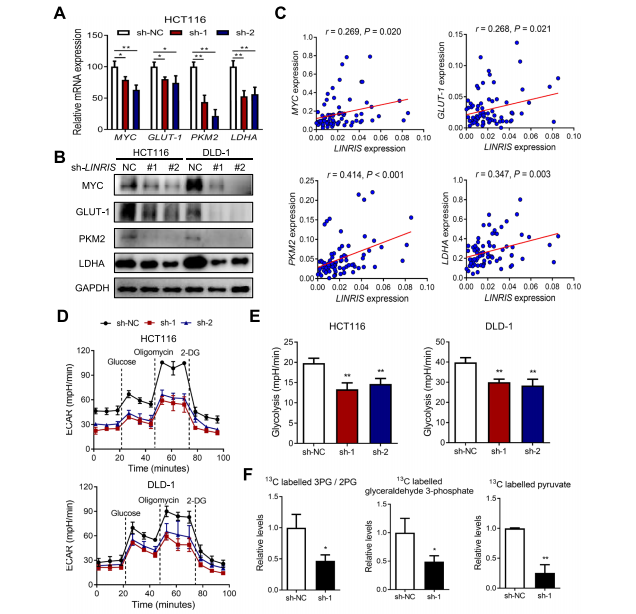
② 回复实验 1:IGF2BP2过表达,可以逆转 sh-LINRIS对细胞增殖活力(BrdU检测,Fig 4G)及细胞糖酵解水平(ECAR检测,Fig 4H-I)的抑制作用。
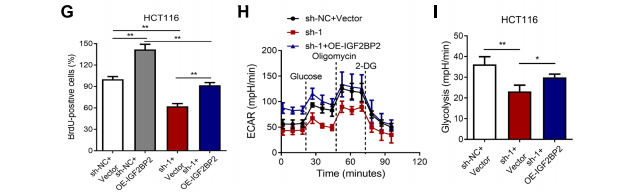

做完前面三步,一段相对完整的机制就验证完整了。差不多达到80分的水平,数据整合整合,差不多够发表一篇5分左右文章了~
第四步,从80到100。往LINRIS-IGF2BP2上游继续深挖机制。
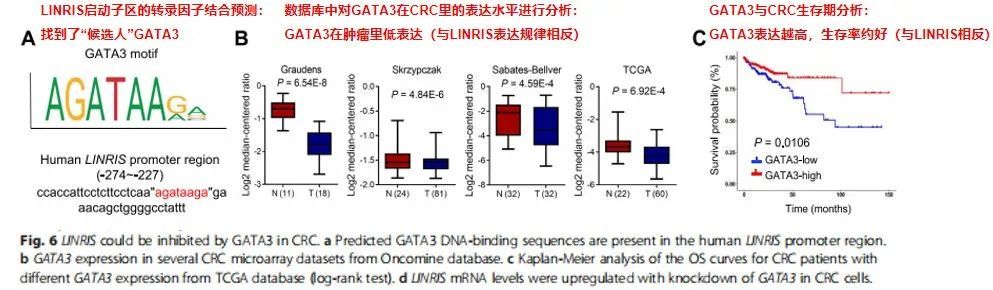 ② 进行细胞验证:首先验证GATA3沉默对LINRIS表达水平的影响(Q-PCR, Fig 6D),然后验证GATA3与LINRIS启动子区的靶向结合关系(CHIP,Fig 6E)。最后证明,GATA3的靶向结合对LINRIS启动子活性的影响(荧光素酶启动子活性检测,Fig 6F-H)。
② 进行细胞验证:首先验证GATA3沉默对LINRIS表达水平的影响(Q-PCR, Fig 6D),然后验证GATA3与LINRIS启动子区的靶向结合关系(CHIP,Fig 6E)。最后证明,GATA3的靶向结合对LINRIS启动子活性的影响(荧光素酶启动子活性检测,Fig 6F-H)。

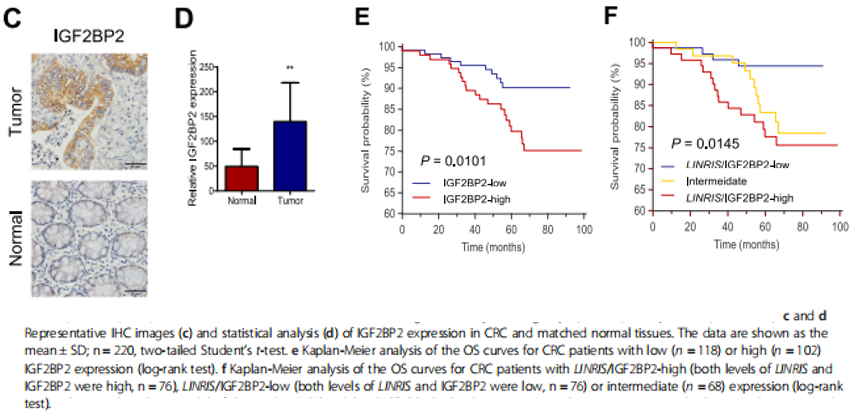
③ 最后临床水平进行验证:Q-PCR(Fig 6I)和IHC(Fig 6J, K)实验证明,临床CRC样本中,GATA3与LINRIS的关系,与①/②部分通过数据库分析 和 细胞水平验证的结论一致。
要想飞升到10分以上,还得往下看~


 综上我们的课题就做(du)完了,最后再华丽丽滴画个假说示例图
综上我们的课题就做(du)完了,最后再华丽丽滴画个假说示例图






