

脓毒症动物模型构建全攻略:CLP vs LPS注射法步骤详解
 2025-04-29 13:50:04
2025-04-29 13:50:04
来源/作者:普拉特泽-生物医学整体课题外包平台
大家好!今天普拉特泽生物继续带大家一起学习新动物模型——脓毒症(Sepsis)是机体对感染反应失调导致的危及生命的器官功能障碍,建立可靠的动物模型对阐明脓毒症发病机制、开发新型治疗策略至关重要。普拉特泽生物将详细对比CLP(盲肠结扎穿孔)和LPS(脂多糖注射)两种最常用的脓毒症建模方法,提供标准化操作流程和实用技巧。
一、CLP模型:临床相关性最高的金标准
1. CLP模型原理与优势
①CLP通过盲肠结扎+穿孔诱导多微生物腹膜炎,最接近临床脓毒症病理过程:
②模拟肠道菌群移位导致的全身炎症反应
③可分级控制疾病严重程度(通过结扎长度和穿孔大小调节)
④适用于脓毒症全程研究(包括高炎症期和免疫抑制期)
2. 标准化操作流程(以C57BL/6小鼠为例)
⑴术前准备
①动物选择:8-12周龄雄性小鼠(雌性激素影响炎症反应)
②禁食处理:术前禁食12小时(不禁水)
③麻醉方案:异氟烷吸入麻醉(2%诱导,1.5%维持)
⑵手术步骤
腹部备皮消毒:10%聚维酮碘溶液消毒
正中切口:约1cm切口暴露盲肠
⑴盲肠处理:
结扎50%盲肠长度(4-0丝线)
21G针头贯通穿刺2次
脏器还纳:轻柔挤压排出少量粪便
关腹缝合:6-0可吸收缝线分层缝合
⑵术后管理:
液体复苏:预热生理盐水(1mL/20g)皮下注射
镇痛:布托啡诺(5mg/kg)每12小时一次
⑶监测指标:
72小时存活率(通常控制在40-60%)
体温(<34℃提示严重脓毒症)
活动度评分(0-5分量表)
3. 关键优化点
穿孔大小控制:21G针头(重度)vs 25G(中度)
菌群预处理:术前3天饮用2%硫酸新霉素可提高一致性
时间窗口:6-12小时(高炎症期)vs 24-72小时(免疫抑制期)
二、LPS模型:简便可控的急性炎症模型
1. LPS模型特点
操作简便:无需手术
高度可重复:剂量依赖性反应
局限性:仅模拟内毒素血症早期炎症阶段
2. 标准化方案
剂量选择(腹腔注射)
严重程度LPS剂量(mg/kg)适用研究
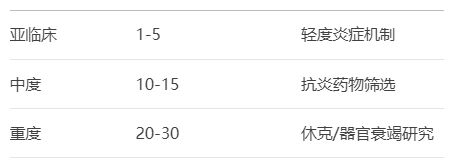
时间进程
①炎症峰值:2-6小时(TNF-α、IL-6)
②器官损伤:12-24小时(ALT/Cr升高)
③恢复期:48-72小时
3. 改良方案
复合模型:LPS+D-半乳糖胺(增强肝损伤)
滴注模型:静脉持续输注(模拟临床进展)
三、CLP与LPS模型对比指南
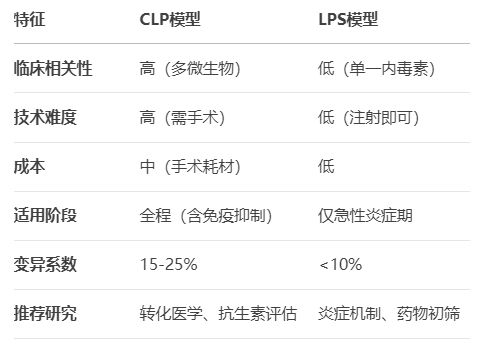
四、模型验证与评价体系
1. 核心检测指标
生理参数:
体温(红外热成像)
呼吸频率(全身体积描记)
血清标志物:
炎症因子(IL-6、TNF-α ELISA)
器官损伤(ALT、Cr、LDH)
组织病理:
肺/肝/肾HE染色
免疫组化(HMGB1、NF-κB)
2. 严重程度分级标准
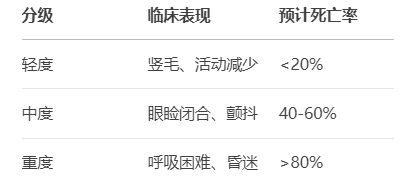
五、常见问题解决方案
⒈CLP术后存活率过高?
增加穿孔直径(改用19G针头)
延长盲肠结扎长度(至75%)
取消术后抗生素
⒉LPS反应不显著?
⑴验证LPS活性(鲎试剂检测)
⑵改用静脉注射(避免腹腔代谢差异)
⑶联合ATP注射(增强NLRP3激活)
⒊模型变异大?
⑴固定手术操作者
⑵使用同批次动物
⑶术前适应性饲养≥7天
六、配套产品推荐
㈠CLP手术套装:
专用手术器械(含微创牵开器)
可吸收缝合线(6-0 PDSⅡ)
㈡检测试剂盒:
脓毒症细胞因子阵列(含IL-1β/6/10/TNF-α)
器官损伤标志物检测(ALT/Cr/BUN联检)
㈢替代模型方案:
粪液注射模型(FIP)
细菌静脉输注系统
结语:模型选择决策树
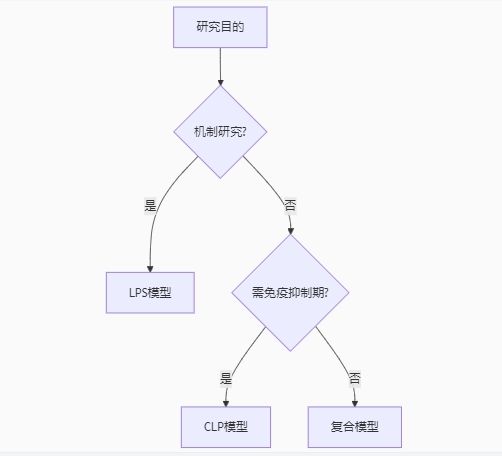
普拉特泽,坚持提供真实、完整、唯一原始数据、原始图片。
普拉特泽生物,自有专业动物房、造模实验室,配套设备齐全,技术团队成熟,熟练掌握各类动物模型构建,更有细胞、分子、病理平台,一站式解决后续相关实验检测。请点击动物实验平台了解详情。

