

【国自然热点文献分享】表观遗传乙酰化
 2021-10-13 14:59:17
2021-10-13 14:59:17
来源/作者:普拉特泽生物-医学整体课题外包
今天,我们跟着今天这篇SCI的思路一起来学习学习吧。
文献题目是:Histone-deacetylase 8 drives the immune response and the growth of glioma. 影响因子7.451分,今年7月份热乎乎的发表在Gliae杂志上。主要研究组蛋白去乙酰化酶8(HDAC8)驱动免疫反应,促进神经胶质瘤的生长。
一、抑制HDAC8降低胶质瘤的生长,延长小鼠的存活期
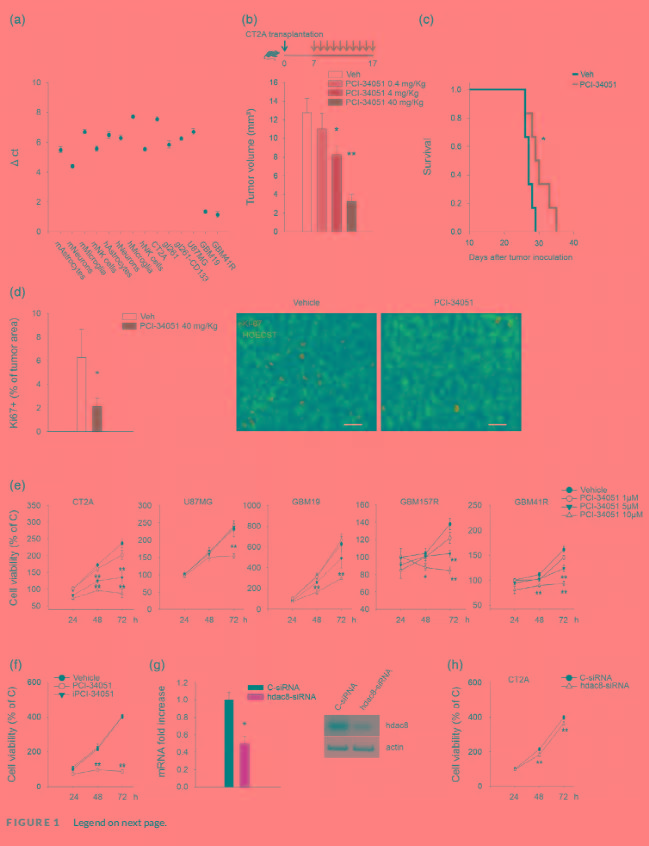
首先,作者在不同的人正常星形胶质细胞系、胶质瘤细胞系、原代胶质瘤细胞、人类神经元来源于诱导的多能干细胞、从癫痫患者样本中分离的小胶质细胞及小鼠胶质瘤细胞中均检测到了HDAC8的表达(Figure 1A)。但是,从患者中获得的原代细胞GBM19和GBM41R中HDAC8表达最高。
接下来,为了研究HDAC8的敲低对胶质瘤发展的影响,作者用HDAC8抑制剂PCI-34051来处理携带胶质瘤的小鼠。发现HDAC8的阻断以浓度依赖的方式减少了胶质瘤的生长(Figure 1B),延长了小鼠的存活时间(Figure 1C),降低了胶质瘤细胞在体内的增殖率(Figure 1D)。
再来看看细胞实验的结果。PCI-34051降低了大部分细胞的增殖能力(Figure 1E)。但,如果在PCI-34051干预细胞的过程中同时用非活性中间体3(iPCI-34051)处理,细胞的增殖能力不受影响(Figure 1F)。用siRNA敲低HDAC8后(Figure 1G),细胞增殖能力也显著降低(Figure 1H)。

二、HDAC8调节α-tubulin蛋白乙酰化驱动胶质瘤细胞迁移和侵袭
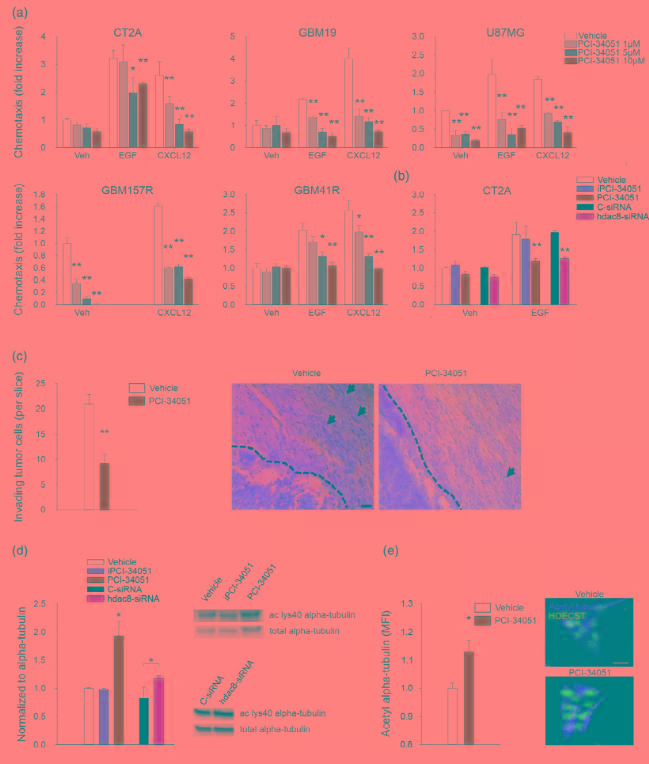
为研究HDAC8的抑制是否能减少胶质瘤细胞迁移从而影响肿瘤生长。作者用不同浓度HDAC8抑制剂PCI-34051下处理人和小鼠的胶质瘤细胞,发现PCI-34051降低了U87MG和GBM157细胞中Veh的表达,同时降低了五株胶质瘤细胞中EGF和CXCL12的表达,即降低了细胞的迁移能力(Figure 2A)。但是,iPCI-34051对肿瘤细胞CT2A无影响效果(Figure 2B),而HDAC8 siRNA的处理降低了CT2A中EGF的表达(Figure 2B)。此外,体内实验发现,PCI-34051的干预降低了肿瘤细胞的侵袭性(Figure 2C)。WesternBlot和免疫荧光实验证实,PCI-34051或HDAC8 siRNA能增加α-tubulin的乙酰化水平(Figure 2D-E)。这些数据表明,抑制HDAC8可减少胶质瘤细胞的迁移和侵袭,并增加α-tubulin的乙酰化。

三、HDAC8调控不同激活状态下小胶质细胞的迁移和形态的动态变化
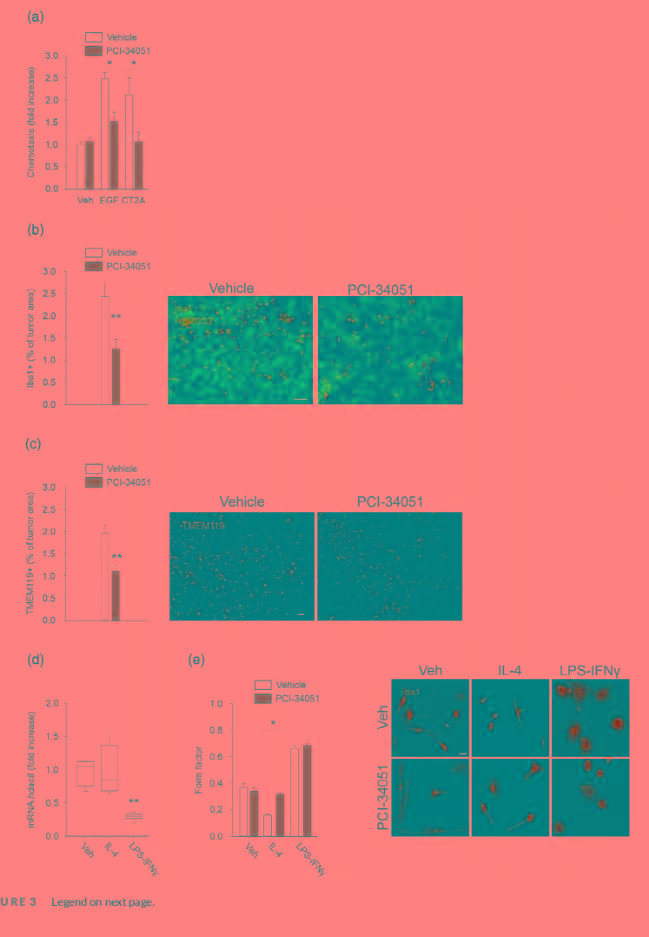
考虑到神经胶质瘤相关的小胶质细胞/巨噬细胞(GAMs)招募到胶质瘤团是支持肿瘤生长的关键机制,作者接下来探讨HDAC8的抑制是否影响GAMs的迁移。 首先,分离原代小鼠胶质细胞。 用PCI-34051干预后发现HDAC8的抑制完全消除了小胶质细胞的趋化性(Figure 3A)。 同时,在用PCI-34051处理的小鼠后发现Iba1+细胞(小胶质细胞/巨噬细胞的标志物)浸润肿瘤肿的数量减少(Figure 3B)。
为了评估骨髓细胞数量的减少是否是由于小胶质细胞的减少导致的,接下来,作者对小胶质细胞特异性标记物TMEM119进行了免疫染色(Figure 3C)。数据显示,抑制HDAC8后,TMEM119+细胞在肿瘤区域减少。
接来下,作者又研究了HDAC8对GAMs表型调节的作用。HDAC8的表达在LPS和IFN-γ刺激下特异性降低(Figure 3D)。阻断HDAC8影响IL-4处理的小胶质细胞的形态学变化(Figure 3E)。
为了进一步研究HDAC8在体内塑造GAMs表型中的作用,从胶质瘤细胞移植后7天开始,用PCI-34051治疗17天。处死小鼠,从同侧或对侧大脑半球分离CD11b+细胞。RT-PCR分析发现肿瘤细胞注射增加了脑胶质瘤半球CD11b+细胞中抗炎基因的表达,并证明PCI-34051治疗完全消除了这种效应,同时增加了促炎基因的表达(Figure 4A)。
体外细胞实验发现,LPS+IFN-γ处理增加了促炎基因的表达,而IL-4增加了抗炎基因的表达(Figure 4B)。用PCI-34051孵育48h,抗炎基因CD163和MMP12的表达降低,促炎基因Nos2和CXCL10的表达增强(Figure 4C)。
综上,HDAC8驱动小鼠和人GAMs向抗炎表型发展。
四、抑制HDAC8可增加胶质瘤细胞中的NKG2D配体,从而增强NK细胞的细胞毒性
作者假设触发NK细胞毒性的NKG2D受体配体的转录受到HDAC8活性的影响。PCI-34051处理CT2A细胞后,CHIP实验发现,ulbp1、h60和raea1基因转录启动子激活标志物三甲基化的组蛋白H3赖氨酸4(H3K4me3)的表达水平显著升高(Figure 5A)。在补充材料中,也可以发现这些基因的转录水平显著增加。
接下来作者进行了NK细胞介导的细胞毒性试验。NK细胞与PCI-34051处理或未处理的CT2A细胞共培养48h,CD107a+的百分比在PCI-34051处理的细胞中显著增加(Figure 5B)。
为了进一步研究依赖于HDAC8的NK细胞毒性活性的分子机制,作者分析了穿孔蛋白PRF1。首先从PRF1敲除的小鼠中分离的NK细胞,与PCI-34051干预或未干预的CT2A细胞共培养。PRF1的缺失消除了HDAC8抑制诱导的NK细胞介导的肿瘤死亡(Figure 5C)。用PCI-34051处理携带胶质瘤的小鼠也得到了类似的结果,活化的CD69+和NKG2D+NK细胞浸润肿瘤肿块的增加,IFN-γ水平无变化(Figure 5D)。
上述结果表明,HDAC8活性在降低NK细胞对胶质瘤细胞的识别和杀伤中起着重要作用。
再捋一捋文章的思路:
第一步,作者发现抑制HDAC8能降低胶质瘤的生成,延长小鼠的生存周期。
第二步,研究发现HDAC8调节α-tubulin蛋白乙酰化从而驱动胶质瘤细胞迁移和侵袭。
第三步,研究HDAC8对GAMs迁移及抗炎表型的调控作用。最后,探讨HDAC8能否触发NK细胞中的NKG2D,从而增强其细胞毒性。
回过头看看,这篇7分多的文章涉及乙酰化研究的内容不多,仅在Figure 2D中用WesternBlot的方法分析了PCI-34051干预后,α-tubulin蛋白乙酰化水平的增加,胶质瘤细胞的迁移和侵袭能力下调。
还没尽兴的伙伴们,静待本月的第二篇与乙酰化相关的文章吧,影响因子翻倍了,会涉及更多关于乙酰化的内容哦。
好啦,那我们今天就讲到这里,如果有更多需要咨询的地方,赶紧戳个关注吧~ 我们不见不散~
- END -
想了解更多的
课题研究与实验手段
请关注我们的推送哟~
