原核重组蛋白表达纯化,是显示组织中纤维的主要方法之一。
普拉特泽生物承接原核重组蛋白表达等病理染色相关服务上万例,积累了操作大量经验,为大家详细分享原核重组蛋白表达纯化问题解析,同时为广大科研工作者开展线上的理论培训与线下实操,可承接蛋白表达实验外包服务
原核重组蛋白表达纯化技术以大肠杆菌(E. coli)为核心表达系统,凭借其培养成本低、繁殖速度快、操作流程标准化等优势,成为生物制药、基础科研、诊断试剂开发等领域制备重组蛋白的核心技术手段。然而,在实际实验操作中,科研人员常面临蛋白表达量过低、杂蛋白污染严重、蛋白可溶性差、目的蛋白降解等技术瓶颈,直接影响实验数据可靠性与项目推进效率。
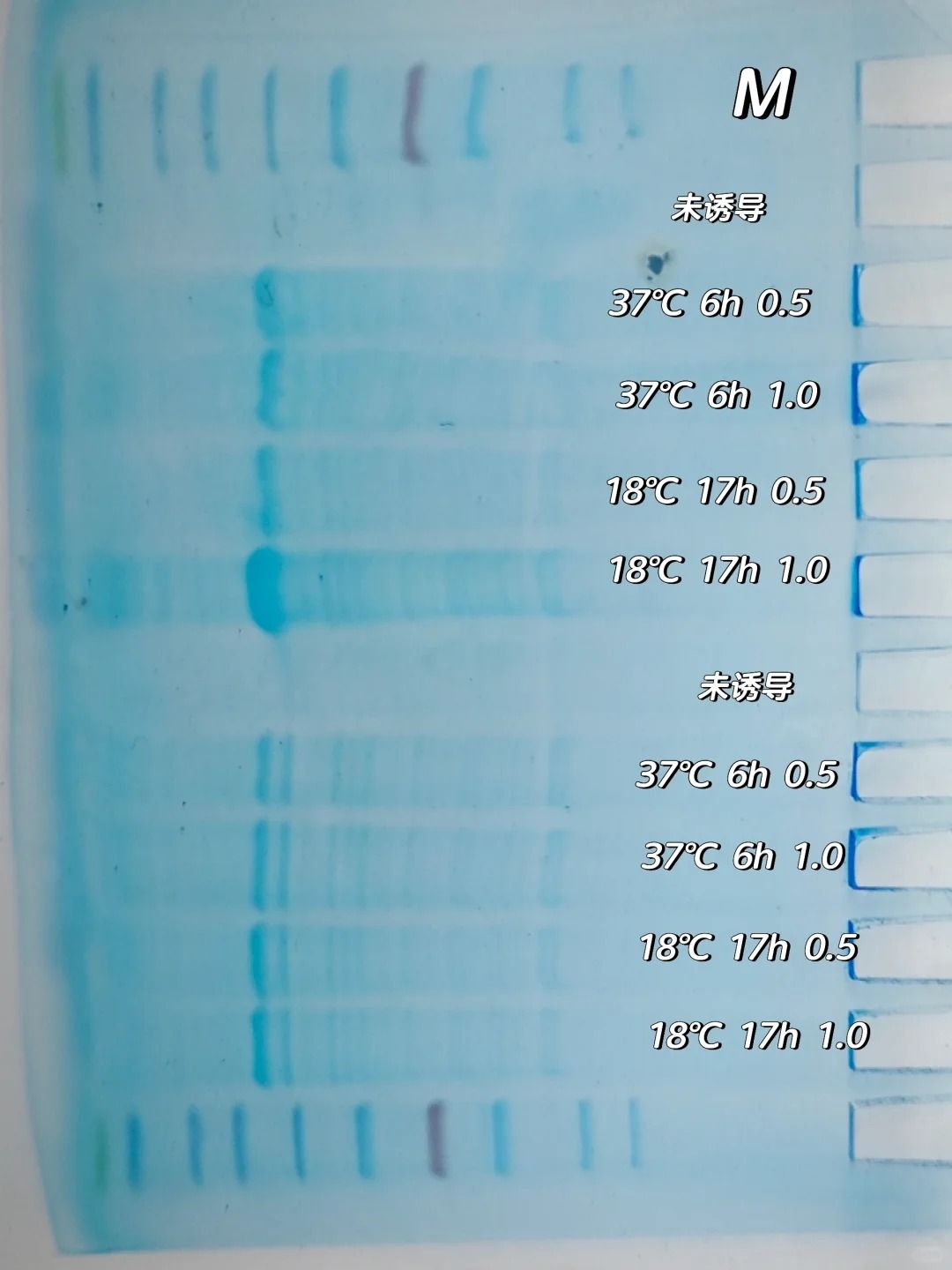
蛋白产量低是原核表达中最高频的问题,其本质是 “目的基因转录效率不足、核糖体结合效率低、宿主代谢负荷失衡” 等多因素共同作用的结果。需从表达系统构建、诱导条件调控、培养体系优化三个维度逐一突破:
载体与菌株的适配性直接决定蛋白表达的 “先天潜力”,若存在配置失衡,即使后续条件优化也难以提升产量:
载体核心元件优化:启动子选择需贴合蛋白特性 —— 强启动子(如 T7、pLac)适合高表达需求,但对毒性蛋白可能导致宿主裂解;弱启动子(如 araBAD、rhaP)可降低基础表达水平,避免目的蛋白对宿主的抑制。同时,核糖体结合位点(RBS)的序列完整性至关重要,需确保其与起始密码子(AUG)间距为 6-8 个碱基,且无二级结构干扰核糖体结合。
密码子偏好性适配:原核生物与真核生物的密码子使用频率存在显著差异,目的基因中的稀有密码子(如大肠杆菌中的 Arg-AGG/AGA、Ile-AUA)会导致翻译停滞。解决方案为:通过生物信息学工具(如 Vector NTI、SnapGene)分析基因序列,对稀有密码子进行同义替换;或选用含稀有密码子 tRNA 补充基因的工程菌株(如 Rosetta (DE3)、BL21-CodonPlus-RIL)。
目的基因完整性验证:载体构建后需通过双酶切和测序确认目的基因插入方向正确、无移码突变或终止密码子提前出现 —— 这是避免 “空载体表达” 或 “截短蛋白表达” 的关键步骤。
亲和层析是原核蛋白纯化的核心手段,标签选择与洗脱条件优化直接决定除杂效果:
标签选择与适配:
His-tag(最常用):与 Ni-NTA 或 Co-NTA 树脂特异性结合,操作简便。若杂蛋白非特异性结合多,可优化:上样前用含 5-20mmol/L 咪唑的平衡液预洗柱子,去除弱结合杂蛋白;洗脱时采用 20-500mmol/L 咪唑梯度洗脱,收集目的蛋白对应的特异性洗脱峰(避免与杂蛋白共洗脱);Co-NTA 树脂对 His-tag 的特异性高于 Ni-NTA,可减少杂蛋白结合。
GST-tag:与谷胱甘肽树脂结合力强,且 GST 标签可提升目的蛋白可溶性,适合难纯化蛋白。纯化后可通过凝血酶(识别 Leu-Val-Pro-Arg-Gly-Ser 位点)切除标签,避免标签对蛋白活性的影响。
MBP-tag:助溶性最强,适合疏水性强的蛋白,纯化后可通过因子 Xa 切除标签。
两步纯化策略:若单一亲和层析纯度不足(如 WB 检测仍有杂带),可采用 “亲和层析 + 离子交换层析” 或 “亲和层析 + 凝胶过滤层析” 组合方案。例如:His-tag 亲和层析初步纯化后,通过离子交换层析(根据蛋白等电点选择阳离子或阴离子树脂)去除电荷差异的杂蛋白;或通过凝胶过滤层析(根据分子量差异)分离目的蛋白与聚合体、小分子杂蛋白,最终纯度可提升至 90% 以上。
标签选择与适配:
His-tag(最常用):与 Ni-NTA 或 Co-NTA 树脂特异性结合,操作简便。若杂蛋白非特异性结合多,可优化:上样前用含 5-20mmol/L 咪唑的平衡液预洗柱子,去除弱结合杂蛋白;洗脱时采用 20-500mmol/L 咪唑梯度洗脱,收集目的蛋白对应的特异性洗脱峰(避免与杂蛋白共洗脱);Co-NTA 树脂对 His-tag 的特异性高于 Ni-NTA,可减少杂蛋白结合。
GST-tag:与谷胱甘肽树脂结合力强,且 GST 标签可提升目的蛋白可溶性,适合难纯化蛋白。纯化后可通过凝血酶(识别 Leu-Val-Pro-Arg-Gly-Ser 位点)切除标签,避免标签对蛋白活性的影响。
MBP-tag:助溶性最强,适合疏水性强的蛋白,纯化后可通过因子 Xa 切除标签。
两步纯化策略:若单一亲和层析纯度不足(如 WB 检测仍有杂带),可采用 “亲和层析 + 离子交换层析” 或 “亲和层析 + 凝胶过滤层析” 组合方案。例如:His-tag 亲和层析初步纯化后,通过离子交换层析(根据蛋白等电点选择阳离子或阴离子树脂)去除电荷差异的杂蛋白;或通过凝胶过滤层析(根据分子量差异)分离目的蛋白与聚合体、小分子杂蛋白,最终纯度可提升至 90% 以上。
蛋白酶抑制剂添加:从菌体破碎到纯化全程,在缓冲液中添加蛋白酶抑制剂 cocktail(含 PMSF、EDTA、抑肽酶等),抑制蛋白酶活性,避免目的蛋白降解产生杂片段。
透析与超滤:洗脱后的蛋白溶液通过透析去除咪唑、高盐等杂质,同时用超滤管浓缩蛋白,减少杂蛋白残留(部分小分子杂蛋白可通过超滤膜筛除)。
原核表达中,由于缺乏真核生物的蛋白折叠辅助系统(如内质网、高尔基体),目的蛋白易错误折叠形成不溶性包涵体,或因疏水性过高导致可溶性降低。需分 “预防策略” 和 “复性挽救” 两步处理:
低温诱导与低浓度诱导剂:16-25℃诱导可延长蛋白折叠时间,0.1-0.3mmol/L IPTG 可降低表达速度,减少错误折叠;
融合可溶性标签:将目的蛋白与 GST、MBP、SUMO 等可溶性标签融合表达,利用标签的亲水性提升蛋白可溶性(如 MBP 标签可使可溶性提升 3-5 倍);
添加折叠辅助因子:在培养基中添加 5%-10% 甘油(维持蛋白构象)、1mmol/L DTT(还原二硫键)、0.5mmol/L GSH/GSSG(氧化还原对,促进正确二硫键形成),或 1mol/L 山梨糖醇(渗透保护剂,减少蛋白聚集)。
若已形成包涵体,可通过 “变性 - 复性” 流程挽救,核心是 “缓慢去除变性剂,给蛋白充足折叠时间”:
包涵体纯化:离心收集菌体后,用含 1% Triton X-100、2mol/L 尿素的洗涤液超声破碎并洗涤 2-3 次,去除包涵体表面吸附的杂蛋白;再通过差速离心(12000rpm,20min)收集纯净包涵体沉淀。
变性溶解:用含 8mol/L 尿素(或 6mol/L 盐酸胍)、10mmol/L DTT 的变性液重悬包涵体,室温孵育 2-4h,使蛋白完全变性(解开错误折叠的二级结构和二硫键)。
逐步复性:采用 “透析复性法”—— 将变性蛋白溶液装入透析袋,依次放入含 6mol/L、4mol/L、2mol/L、1mol/L、0mol/L 尿素的复性液中,每步透析 4-6h,逐步降低变性剂浓度;复性液中需添加 50mmol/L Tris-HCl(pH8.0)、150mmol/L NaCl、1mmol/L GSH/GSSG(氧化还原对),促进正确二硫键形成。
复性后纯化:复性后的蛋白溶液通过亲和层析纯化,去除未复性的聚集蛋白和杂蛋白,获得可溶性目的蛋白。
全程低温操作:菌体破碎、离心、纯化等步骤均在 4℃或冰浴条件下进行,降低蛋白酶活性;
选用蛋白酶缺陷型菌株:如 BL21 (DE3) pLysS 菌株,可表达 T7 溶菌酶,抑制未诱导时的基础表达,减少目的蛋白提前合成并降解;
优化缓冲液 pH:根据蛋白特性调整缓冲液 pH(多数蛋白在 pH7.0-8.0 时稳定性最佳),避免酸性或碱性条件导致蛋白构象变化,降低降解风险。
验证折叠正确性:通过圆二色谱检测蛋白二级结构(α- 螺旋、β- 折叠比例),或凝胶过滤层析分析蛋白均一性(单体比例>90% 为合格),判断是否因折叠错误导致无活性;
切除融合标签:若标签(如 His-tag、GST-tag)遮挡蛋白活性位点,可通过特异性蛋白酶切除标签后再检测活性;
考虑真核表达系统:若目的蛋白依赖真核生物的翻译后修饰(如糖基化、磷酸化、棕榈酰化),原核表达无法实现活性折叠,需切换至酵母(Pichia pastoris)、昆虫细胞(Sf9)等真核表达系统。
预防措施:培养基 121℃高压灭菌 20min,接种用枪头、离心管等耗材提前灭菌;超净台使用前紫外线消毒 30min,操作时佩戴无菌手套和口罩;
污染排查:若菌液浑浊速度异常(<6h 达到 OD600>1.0)或出现异味,取 10μL 菌液涂 LB 平板,37℃培养 12h,观察菌落形态 —— 若出现多种菌落形态,说明存在杂菌污染;
处理方案:丢弃污染菌液,更换新的菌种(从 - 80℃冰箱复苏原始菌种)和培养基,重新接种培养。
高效的蛋白制备需遵循 “先筛选、再优化、后纯化” 的逻辑:
预实验筛选:构建 2-3 种载体 - 菌株组合(如 T7 启动子 + BL21 (DE3)、T7 启动子 + Rosetta (DE3)),小体积(5mL)培养并诱导,通过 SDS-PAGE 筛选表达量最高、可溶性最好的组合;
表达条件优化:针对筛选出的组合,梯度测试诱导温度、诱导剂浓度、诱导时间,确定最佳表达参数;
纯化策略制定:根据蛋白标签选择亲和层析方法,若纯度不足,添加第二步纯化(离子交换或凝胶过滤);
活性验证与调整:纯化后通过 ELISA、Western Blot、酶活测定等方法验证蛋白活性,反向优化表达或纯化条件。
原核重组蛋白表达纯化的核心是 “针对性优化”—— 结合目的蛋白的分子量、疏水性、毒性等特性,精准调整实验参数,同时注重操作细节(如无菌环境、低温条件)。通过本文的问题拆解与解决方案,可有效突破低产量、高杂蛋白、低活性等技术瓶颈,提升蛋白制备效率与质量,为后续科研或产业化应用奠定基础。
今天关于原核重组蛋白表达纯化常见问题深度解析就分享到这儿啦~如果您在实验过程中遇到技术问题,或者需要实验外包和代做,可与我们技术老师联系18570028002(微信同号)



 2025-10-24 17:37:58
2025-10-24 17:37:58


